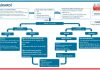
Spontan dolaşımın başarılı bir şekilde geri dönmesi, kardiyak arrestten tam olarak derlenmenin sadece ilk adımıdır. Kardiyak arrest sonrası beyin hasarı oluşması, miyokard disfonksiyonu, sistemik iskemi / reperfüzyon yanıtı ve kalıcı patolojiyi içeren post-kardiyak arrest sendromu sıklıkla resüsitasyondan sonraki dönemi karmaşık hale getirir.366 Post-kardiyak arrest sendromunun şiddeti ve arrestin nedenine bağlı olarak pek çok hastada resüsitasyon sonrası bakım dönemi boyunca çoklu organ desteği ve tedavisi gerekebilir. Bu durum özellikle nörolojik iyileşmenin kalitesini ve sağkalım sonuçlarını belirler.367-373 Resüsitasyon sonrası bakım algoritması (Şekil 1.15), bu hastalarda sağkalımın optimize edilmesi için gerekli bazı anahtar girişimleri göstermektedir.
Post-kardiyak arrest sendromu
Post-kardiyak arrest sendromu; kardiyak arrest sonrası beyin hasarı, myokard disfonksiyonu, sistemik iskemi/reperfüzyon yanıtı ve tetikleyen ısrarcı patolojiden meydana gelir.366,374,375 Bu sendromun ciddiyeti kardiyak arrestin süresi ve nedenine göre değişiklik göstermektedir. Kardiyak arrest kısa süreli ise hiç görülmeyebilir. Kardiyovasküler yetmezlik ilk üç gün içindeki ölümlerin çoğundan sorumlu iken, beyin hasarına bağlı ölümlerin çoğu daha sonraki günlerde oluşur.376-378 Prognozu kötü olan hastalarda, ölümlerin çok büyük oranı (yaklaşık %50’si) destek tedavisinin geri çekilmesi nedeniyle olur;378,379 bu nedenle prognoz planının önemi vurgulanmalıdır (altta görülen). Kardiyak arrest sonrası beyin hasarı oluşması mikrodolaşım yetersizliği, otoregülasyonda bozulma, hipotansiyon, hiperkarbi, hipoksemi, hiperoksi, pireksi, hipoglisemi, hiperglisemi ve nöbetlerle kötüleşebilir. Kardiyak arrest sonrasında belirgin miyokard disfonksiyonu sıktır, tipik olarak 2-3 günde düzelir, ancak tam düzelme belirgin olarak daha uzun sürebilir.380-382 Kardiyak arreste bağlı tüm vücut iskemi/reperfüzyonu, çoklu organ yetmezliğine katkıda bulunan ve enfeksiyon riskini arttıran immünolojik ve koagülasyon yolaklarını aktive eder.383 Bu nedenle, post-kardiyak arrest sendromu ile sepsis arasında intravasküler volüm açığı, vazodilatasyon, endotel hasarı ve mikrodolaşım bozuklukları gibi bir çok ortak nokta vardır.384-390
Hava yolu ve solunum
Hipoksemi ve hiperkarbinin her ikisi de yeni kardiyak arrest gelişme olasılığını artırır ve sekonder beyin hasarına katkıda bulunabilirler. Birkaç hayvan çalışması, hiperokseminin
Şekil 1.15. Resüsitasyon sonrası bakım algoritması. SKB – Sistolik kan basıncı; PKG – perkütan koroner girişim; BTPA – Bilgisayarlı tomografi pulmoner anjiyogram, YBÜ – Yoğun bakım ünitesi; OAB – ortalama arter basıncı; ScvO2 – santral venöz oksijenasyon; EEG – elektroensefalogram; ICD – implante edilen kardiyoverter defibrilatör.
erken dönem SDGD sağlanmasından sonra oksidatif strese neden olduğunu ve post-iskemik dönemde nöronlara zarar verdiğini göstermektedir.391 Tüm insan çalışmaları yoğun bakım verilerinden alınmış olup, kardiyak arrestte resüsitasyon sonrası hiperokseminin potansiyel etkileri konusunda karmaşık sonuçlar yaratmıştır.392 Yakın zamanlı ve ST elevasyonlu miyokard enfarktüsünde hava ve oksijen desteğini karşılaştıran bir çalışmada, oksijen desteğinin miyokardiyal hasarı, miyokard enfarktüsü tekrarlama riskini ve majör kardiyak aritmileri ve 6. aydaki büyük enfarkt alanı ile ilişli olduğu gösterilmiştir.393 Kardiyak arrestten sonra nörolojik hasarı arttırma olasılığı ve miyokard enfarktüsünden sonra zararı kanıtlandığından, kanın oksijen satürasyonu güvenle monitörize edilir edilmez (kan gazı analizi ve/veya puls oksimetre ile), arter kanı oksijen satürasyonunu %94-98 arasında idame ettirecek şekilde inspire edilen oksijen konsantrasyonu titre edilmelidir. Hipoksemi de zararlı olduğundan hipoksemiden sakının; inspire edilen oksijen konsantrasyonunu azaltmadan önce, arteriyal oksijen satürasyonun doğru ölçüldüğünden emin olun.
Beyin fonksiyonu bozulmuş her hastada trakeal entübasyonu, sedasyonu ve kontrollü ventilasyonu düşünün. Kardiyak arresten sonra, hiperventilasyon ile hipokapni oluşur ve serebral iskemiye neden olur.394-
396 Kardiyak arrest kayıtları kullanılarak yapılan gözlemsel çalışmalar, hipokapni ile kötü nörolojik sonuç arasında ilişki saptamıştır.397,398 Prospektif veriler elde edilene kadar, normokarbiyi sağlayacak şekilde ventilasyonu ayarlamak ve bunu “end-tidal” CO2 ve arteriyel kan gazı değerleri ile monitörize etmek uygundur.
Dolaşım
Akut koroner sendrom (AKS), hastane dışı kardiyak arrestlerin en sık nedenlerinden biridir: yakın zamanda yayınlanan bir meta-analizde; non-kardiyak etiyoloji gözlenmeyen HDKA hastalarında akut koroner arter lezyonu prevelansı %59-71 oranında saptanmıştır.399 Pek çok gözlemsel çalışma, kardiyak arrestten sonra SDGD sağlanan hastalarda erken perkütan koroner girişimi kapsayan acil kardiyak kateterizasyon laboratuvar değerlendirmesinin uygun olduğunu göstermiştir.400,401 Bu hastalarda invazif girişim (yani erken koroner anjiyografiyi takiben gerekirse acil PKG), özellikle uzamış resüsitasyona ve nonspesifik EKG değişikliğine sahip olanlarda, spesifik kanıtların olmaması ve kaynakların kullanımındaki (PKG merkezlerine hastaların transferini kapsayan) belirgin etkileri nedeniyle tartışmalıdır.
ST-elevasyonu olan SDGD izleyen perkütan koroner girişim
Eldeki veriler temelinde, EKG’de ST-elevasyonu olan ve kardiyak orijinli olduğu şüphelenilen hastane dışı erişkin kardiyak arrest hastalarında SDGD sağlanırsa acil kardiyak kateterizasyon laboratuvarı değerlendirilmesi (gerektiğinde acil PKG) gerçekleştirilmelidir. Bu öneri, seçilmiş popülasyondan elde edilen güçlü olmayan kanıtlara dayanır. Gözlemsel çalışmalarda HDKA sonrasında optimal sonuçların PKG ve TTM kombinasyonu ile birlikte sağlandığı belirlenmiştir; bu girişimler nörolojik açıdan iyi sağkalımın geliştirilmesi stratejilerinin parçası olan standardize post-kardiyak arrest protokollerinde yer alabilir.401-403
ST-elevasyonu olmayan SDGD izleyen perkütanöz koroner girişim
Kardiyak kökenli olmayan arrest hastalarındaki AKS’un genel bulgularının aksine, kardiyak arrest hastalarında koroner iskeminin değerlendirilmesine yönelik standart ölçütler daha az hassastır. Alışılmış klinik verilerin, EKG ve spesifik markerların HDKA nedeni olarak bir koroner arter oklüzyonunu tespit etmedeki sensitivite ve spesifitesi belli değildir.404-407 Bazı geniş gözlemsel serilerde HDKA olan ve SDGD sağlanan hastalarda, ST elevasyonu olmadan AKS olabileceği gösterilmiştir.408-411 Bu grup ST elevasyonu olmayan hastalar, gözlemsel çalışmaların verilerine göre, acil kardiyak kateterizasyon laboratuvarı değerlendirilmesinden potansiyel yarar görür. 410,412,413 Kardiyak arrest için koroner neden açısından çok yüksek risk taşıyan hastalarda SDGD sağlanırsa acil kardiyak kateterizasyon laboratuarı için değerlendirilme ve tartışma yapılması akla uygundur. Hastanın yaşı, KPR süresi, hemodinamik instabilite, mevcut kardiyak ritim, hastaneye ulaştığındaki nörolojik durum, mevcut olan kardiyak etiyoloji gibi faktörler girişimlere akut dönemde başlama ya da hastane yatışına dek erteleme kararını vermeyi etkiler.
Komputerize tomografi (CT) çekiminin zamanlaması ve endikasyonları
HDKA’in kardiyak nedenleri son yıllarda geniş çaplı olarak araştırılmasına rağmen non-kardiyak nedenler hakkında bilinenler azdır. Solunumsal veya nörolojik bir nedenin erken tespit edilmesi, optimal bakım için hastanın spesifik bir yoğun bakım ünitesine naklini sağlayabilir. Prognoz hakkında bilginin artması TTM gibi özellikli tedavileri uygulama konusunda tartışmayı sağlar. Solunumsal veya nörolojik bir nedenin erken tanınması, hastaneye kabulde beyin ve göğüs BT görüntülemenin, koroner anjiyografiden önce yapılmasını gerçekleştirir. İleri sürülen nörolojik veya solunumsal nedene ait bulgu ve semptomların yokluğunda (örn. nörolojik hastalar için başağrısı veya konvülsiyon, bilinen ve kötüleşen solunumsal hastalığı olan hastalarda nefes darlığı veya hipoksi gibi) veya miyokardiyal iskeminin EKG veya klinik bulgusu var ise, ilk önce koroner anjiyografi çekilir, daha sonra BT görüntüleme yapılır. Bazı olgu serileri, hastaların önemli bir oranında, non-kardiyak arrest nedenlerinin tanısını koymak için bu stratejinin kolaylık sağladığını göstermiştir.358,414
Hemodinamik yönetim
Kardiyak arrest sonrası miyokard disfonksiyonu; hipotansiyon, düşük kardiyak indeks ve aritmilerle karakterize hemodinamik instabiliteye neden olur.Tüm hastalarda erken dönem ekokardiyografi yapılması, miyokardiyal disfonksiyonun tespiti ve derecesinin tayini için önemlidir.Post-resüsitasyon miyokardiyal disfonksiyon sıklıkla, en azından geçici olarak inotropik destek gerektirir.
Kan basıncı, kalp atım hızı, idrar çıkışı, plazma laktat klirensi, santral venöz oksijen satürasyonu, tedavide kılavuz olabilir. Özellikle hemodinamik olarak stabil olmayan olan hastalarda, seri olarak ekokardiyografi kullanılabilir. YB’da sürekli kan basıncı monitörizasyonu için arter kanülasyonu gereklidir.
Bazı yakın zamanlı çalışmalardaki tartışmalara rağmen,kardiyak arrest sonrası tedavi stratejisinde,370spesifik kan basıncını hedefleyen tedaviyi de içeren sepsis demetlerindeki gibi, erken hedefe yönelik tedavi önerilmektedir. Kesin veriler bulunmadığında, hastanın normal kan basıncını, kardiyak arrestin nedeni ve
miyokard disfonksiyonunun derecesini dikkate alarak, yeterli bir idrar çıkışı (1 ml /kg/ st) sağlayacak ve normal veya azalan plazma laktat değerleri elde edecek şekilde bir ortalama arter kan basıncı hedefleyiniz. Bu hedefler, eşlik eden hastalıklar ve bireysel fizyolojik temele dayandığından değişken olabilir. Hipotermi idrar atılımını artırabilir ve laktat klirensini bozabilir.
Vücuda yerleştirilebilir kardioverter defibrilatörler
Primer bir koroner olaydan 24-48 saat sonra gelişen ventriküler aritmiden dolayı resüsite edilmiş, belirgin sol ventrikül disfonksiyonu olan iskemik hastalarda, vücuda yerleştirilebilir kardiyoverter defibrilatör uygulamayı düşünün.
Disabilite (Nörolojik derlenmeyi optimize etmek)
Beyin perfüzyonu
Hayvan çalışmaları, SDGD sağlandıktan hemen sonra, kısa süreli multifokal serebral yeniden akım olmayan devreyi takiben 15-30 dk süreli geçici global serebral hiperemi olduğunu göstermektedir. Bu devreyi serebral oksijen metabolizma hızı kademeli olarak iyileşirken 24 saate kadar olan serebral hipoperfüzyon takip eder. Asfiksik kardiyak arrestlerde, SDGD sağlandıktan sonra geçici olarak beyin ödemi oluşur, fakat klinik olarak intrakranial basınçtaki artış ile çok nadiren ilişkilidir. Pek çok hastada, bazı kardiyak arrestlerden sonra serebral kan akımının otoregülasyonu yetersizdir (yoktur veya sağa kaymıştır); bunun anlamı, serebral perfüzyon nöronal aktivite linklerine bağlı olmak yerine, serebral perfüzyon basıncı ile sağlanır. Bu yüzden, SDGD sağlandıktan sonra, ortalama arter basıncı, hastanın normal seviyelerinde tutulmalıdır.
Sedasyon
SGDG sağlandıktan sonra en az 24 saat süreyle hastaların sedasyon ve ventilasyonu sık olarak uygulanmasına karşın, kardiyak arrest sonrasında ventilasyon, sedasyon ve nöromusküler blokaj dönemini tanımlayan yüksek değerlilikte veri yoktur.
Nöbetlerin kontrolü
Kardiyak arrest sonrası nöbetler sıktır ve SDGD sağlanan komadaki hastaların yaklaşık üçte birinde görülür. Miyokloni en yaygınıdır ve %18-25 oranında görülür, geri kalanı fokal veya jeneralize tonik-klonik kasılmalar şeklindedir veya her iki tipi bir arada görülebilir.434 Klinik olarak nöbetler, miyokloni de dahil olmak üzere epileptik orijinli olabilir veya olmayabilir. Diğer motor aktiviteler yanlışlıkla konvülsiyon sanılabilir ve miyokloninin birkaç tipi vardır, çoğu non-epileptiktir. Klinik olarak nöbet aktivitesi olan hastalarda, epileptik aktiviteyi saptamak için aralıklı elektroensefalografi (EEG) kullanın. Tedavinin etkileri ve status epileptikus tanısı için hastaları sürekli EEG ile monitörize etmeyi düşünün. Konvülsiyonlar, serebral metabolik hızı arttırabilir, kardiyak arrestten kaynaklanan potansiyel beyin hasarını arttırır; sodyum valproat, levetiracetam, fenitoin, benzodiazepinler, propofol veya barbitürat ile tedavi edin. Miyokloni tedavisi özellikle zor olabilir; fenitoin sıklıkla etkisizdir. Propofol post-anoksik miyokloniyi baskılamada etkilidir.
Klonazepam, sodyum valproat ve levetiracetam post-anoksik miyoklonide etkili olabilecek antimiyoklonik ilaçlardır.
Glukoz kontrolü
Kardiyak arrestte resüsitasyondan sonra yüksek kan glukozu ile kötü nörolojik sonuçlar arasında güçlü bir ilişki vardır. Mevcut verilere göre SDGD sağlanmasından sonra kan glukozu ≤10 mmol/ l’de (180 mg/dl) idame ettirilmeli ve hipoglisemiden kaçınılmalıdır. Sıkı glukoz kontrolü kardiyak arrest sonrasında spontan dolaşımı geri dönen erişkin hastalarda artmış hipoglisemi riski nedeniyle uygulanmamalıdır.
Sıcaklık kontrolü
Kardiyak arrest sonrası ilk 48 saatte hipertermi (hiperpireksi) periyodu sıktır. Bazı çalışmalar kardiyak arrest sonrası pireksi ve kötü sonuçlar arasındaki ilişkiyi ortaya koymuştur. Sıcaklık artışının sonuç üzerine olan etkisi kanıtlanmamış olsa da, kardiyak arrest sonrasında görülen hipertermiyi antipiretik veya aktif soğutma ile tedavi etmek mantıklıdır.
Hayvan ve insan verileri ılımlı hipoterminin nöroprotektif olduğunu ve yaygın beyin hipoksi-iskemi periyodundan sonra sonucu iyileştirdiğini göstermektedir. Kardiyak arrestten sonra uygulanan tüm terapötik hipotermi çalışmaları sadece komadaki hastaları içermektedir. Bir randomize çalışma ve bir psödo- randomize çalışma, hastane dışı VF kardiyak arrest sonrası komada kalan hastalarda uygulanan hipoterminin hastaneden taburcu olmada veya altıncı ayda iyi nörolojik sonuçlar elde etmede etkili olduğunu göstermiştir.Soğutma, SDGD sağlandıktan sonra dakikalar ve saatler içinde başlatılmış ve 32-34oC’lik sıcaklık sınırları 12-24 saat boyunca devam ettirilmiştir.
Hedefe yönelik hipotermi (TTM) çalışmasında; HDKA olan tüm ritimlerdeki 950 hasta; 33oC veya 36oC olacak şekilde 36 saatlik sıcaklık kontrolü için (hedeflenen sıcaklığa 28 saatte ulaştıktan sonra yavaş geri ısıtma) randomize edildi.Prognoz belirleme ve yaşam destek tedavisini geri çekmeyi belirlemek için sıkı takip protokolleri uygulandı. Tüm mortalite nedenleri içinde, primer sonuçlarda farklılık yoktu, 6 ay içindeki nörolojik sonuçlar benzerdi (çalışma sonundaki mortalite için hazard oranı (HR) 1.06, % 95 CI 0.89-1.28; ilk altı aydaki kötü nörolojik sonuç veya ölüm için rölatif risk (RR) 1.02, %95 CI 0.88-1.16). Altıncı aydaki detaylı nörolojik sonuçlar benzerdi. Önemli olarak, çalışmaya alınan her iki koldaki hastaların sıcaklıkları iyi kontrol edildi, her iki grupta da vücut sıcaklığının yükselmesi engellendi.
Hedefe yönelik sıcaklık yönetimi veya sıcaklık kontrolü tanımları yerine terapötik hipotermi tanımı tercih edilmiştir. ILCOR’un İYD çalışma grubu hedefe yönelik hipotermi tedavisinde175 bazı öneriler sunmuştur ve bunlar da ERC kılavuzunda yer almıştır:
-
Sıcaklık kontrolü uygulanan hastalarda hedef sıcaklığı 32oC ve 36oC arasında sabit bir değerde tutun (kuvvetli öneri, orta-kalitede kanıt).
-
Kardiyak arrest hastalarının belirli alt çalışma gruplarında düşük (32-34oC) veya yüksek (36oC) sıcaklıklarından hangisinin daha yararlı olup olmadığı tam bilinmemektedir, bu elemeyi yapmak için daha ileri araştırmalar yardımcı olabilir.
-
TTM, HDKA olup ve başlangıç ritmi şok uygulanan arrest ritmi olan ve SDGD sağlanan, bilinci kapalı erişkin hastalara önerilir (kuvvetli öneri, düşük-kalitede kanıt)
-
TTM, HDKA olup ve başlangıç ritmi şok uygulanmayan arrest ritmi olan ve SDGD sağlanan, bilinci kapalı erişkin hastalara önerilir (zayıf öneri, çok düşük-kalitede kanıt)
-
TTM, HİKA olup ve başlangıç ritmi herhangi bir arrest ritmi olan ve SDGD sağlanan, bilinci kapalı erişkin hastalara önerilir (zayıf öneri, çok düşük-kalitede kanıt)
-
Eğer TTM uygulanacak ise, bu süre en az 24 saat olmalıdır (daha önceki iki büyük RKÇ’da belirtildiği üzere) (zayıf öneri, çok düşük kalitede kanıt)
Sıcaklık kontrolü ne zaman?Hangi hedef sıcaklık seçilirse, aktif sıcaklık kontrolünü gerçekleştirmek ve bu düzeyde sıcaklık idamesi sağlamak gerekir. Daha önceki öneriler, SDGD sağlandıktan hemen sonra mümkün olan en kısa sürede soğutma başlanmalıdır şeklindeydi ki, bu öneri sadece klinik öncesi veri ve rasyonel olasılıklara dayanmaktaydı. Hayvan çalışmaları, SDGD sağlandıktan sonra ne kadar erken soğutmaya başlanırsa, o kadar iyi sonuçlar alındığını göstermektedir. Spontan olarak daha hızlı soğutulan hastalarda, daha kötü nörolojik sonuçlar ile bir ilişki olduğu gerçeği belirtilmesinden dolayı gözlemsel çalışmalar ile ilgili kafa karışıklığı vardır.En şiddetli nörolojik hasarlı olanların, beden sıcaklık kontrol yeteneğinin kaybedilmesine daha fazla eğimli oldukları hipotez olarak ileri sürülmüştür.
SDGD sağlandıktan hemen sonra hastane öncesinde büyük hacimlerde soğuk intravenöz sıvının hızla verilmesinin, hastaneye yatışa dek geciktirilmesi ile karşılaştırıldığı randomize çalışmada nakil sırasında tekrar arrest ve akciğer ödemi daha fazla görülmüştür.Hastane öncesi kontrolsüz soğuk sıvı infüzyonu önerilmese de, hastalar çok iyi monitörize edildiyse ve hedef olarak düşük sıcaklık (33oC gibi) amaçlandı ise, soğuk intravenöz sıvıların infüzyonu hala mantıklı olabilir. Soğuk intravenöz sıvıların büyük hacimlerde hızlı infüzyonu haricindeki diğer erken soğutma stratejileri ve hastane öncesinde KPR sırasında soğutma henüz yeteri kadar çalışılmamıştır.
Sıcaklık nasıl kontrol edilir? Bugüne kadar, herhangi bir spesifik soğutma tekniğinin diğer tekniklerle karşılaştırıldığında yaşam şansını arttırdığına yönelik kesin kanıt yoktur; fakat internal kullanılan aletlerin, eksternal teknikler ile karşılaştırıldığında daha kesin sonuçlara yol açtığı kabul edilmektedir.Rebound hipertermi, kötü nörolojik sonuç ile ilişkilidir.Bu nedenle, yeniden ısıtma da yavaşça yapılmalıdır; optimal hız bilinmemektedir, ancak günümüzdeki uzlaşı saatte yaklaşık 0.25-0.50oC ısıtma şeklindedir.
Prognozun belirlenmesi
Prognozun belirlenmesi ile ilgili bu bölüm, 2015 kılavuzunun öngördüğü, ESICM’in TEM’ın ERC İYD Çalışma Grubu üyelerinin yazmış olduğu, kardiyak arrestin komada sağkalan grubunda Nörolojik Prognoz Belirlemenin Danışma Beyanatlarındanuyarlanmıştır.
Kardiyak arrest resüsitasyonundan sonra hipoksik-iskemik beyin hasarı yaygındır. Hastane dışı kardiyak arrestleri takiben yoğun bakıma alınma öncesinde ve sonrasında terapötik hipotermi uygulansa da, ölen hastaların üçte ikisinin nörolojik hasar nedeniyle kaybedildiği gösterilmiştir. Bu ölümlerin çoğu, kötü nörolojik prognoz belirlenmesi sonucu, sunulan tedavinin geri çekilmesi nedeniyle olmaktadır. Bu nedenle, kardiyak arrest sonrası resüsite edilip dönen komatöz hastalar değerlendirildiğinde, yanlış kötümser tahminlerin minimal riskli olması esastır. İdeal olanı, kötü prognoz saptandığında, yalancı pozitiflik oranının (FPR), en yakın olası güvenlik intervali ile birlikte (CI) sıfır olmasıdır.
Fakat, prognoz belirleyici çalışmalar, oldukça az hastayı kapsar, FPR % 0 olsa ise bile, CI % 95’in üzerinde olduğu durumlar oldukça sıktır. Dahası, birçok çalışma kendi sonuçları-tahminleri ile de çatışmıştır, tedavi eden hekim sonuçlara yanıtsız olamadığında kendi içinde taraf olur ve bunlar da tedaviyi devam etme veya sonlandırma kararında etkili olmaktadır. Sonuçta, tek başına hedefe yönelik hipotermi ve sedatifler ikisi birlikte veya nöromüsküler bloker ilaçlar idamede kullanılması ile, özellikle klinik değerlendirme temelinde prognoz belirleyici endekslerle etkileşme potansiyeli olabilir. Prognoz belirlemede multimodal uygulama esastır ve klinik değerlendirme, elektrofizyoloji, biyomarker’lar ve görüntülemeyi içerir.
Şekil 1.16. Prognoz belirleme stratejisi algoritması. EEG – elektroensefalografi; NSA – nöron spesifik enolaz; SSEP – somatosensoriyal uyarılmış potansiyeller; SDGD – spontan dolaşımın geri dönmesi; M – Glasgow koma skalasında motor yanıt; YPO – yanlış pozitiflik oranı; GA – güven aralığı.
Kardiyak arrestten sonra komadaki hastanın prognozu için dikkatli bir klinik nörolojik muayene esastır.473Günlük klinik muayene ile amaca yönelik hareketlerin olup olmadığı ya da beyin ölümü lehine klinik bulgu gelişip gelişmediği saptanmalıdır.
Global post-anoksik hasarlanmayı izleyen beyin iyileşme süreci, çoğu hastada arrestten sonraki 72 saat içinde tamamlanır. Fakat, SDGD sağlandıktan sonra 72 saat içinde, 12 saate kadar sedatif almış olan hastalarda, nörolojik muayene için klinik değerlendirmenin güvenirliği azalabilir. Karar vermeden önce, en büyük yanıltıcı olabilecek; sedasyon ve nöromüsküler blokaj, hipotermi, ciddi hipotansiyon, hipoglisemi, metabolik ve solunumsal düzensizlikler dışlanmış olmalıdır.Sedatif ve nöromüsüler bloker ilaçlar uzun süreden sonra kesildiğinde, klinik muayeneyi etkilemesinden sakınılmalıdır. Mümkün ise, kısa etkili ilaçlar tercih edilir. Rezidüel sedasyon/paraliziden endişe ediliyor ise, bu ilaçların etkileri antidotları kullanarak değerlendirilmelidir.
Prognoz belirleme algoritması (Şekil 1.16) SDGD sağlandıktan sonra 72 saat içinde ekstensör motor yanıtı olan veya olmayan komadaki tüm hastalara uygulanabilir. Daha erken prognoz belirleyen testlerin sonuçları, bu dönemde birlikte değerlendirilir.
İlk önce en doğru bilgileri değerlendirin. Bu bilgiler yüksek spesifisite ve doğruluk oranına sahiptir (FPR <% 5 ile % 95, Cis <%5 olan kontrollü sıcaklık ile tedavi olan hastalar) ve en az üç farklı grup araştırmacı tarafından birkaç çalışmada dökümante edilmiştir. Bunlar, SDGD sağlandıktan 72 saat sonra, bilateral pupiller refleksi olmayanlar ve ısınmadan sonra N20 dalga somatosensoriyal uyarılmış potansiyel yanıtı (kontrollü ısı ile tedavi edilmeyen hastalarda SDGD sağlandıktan 24 saat sonra bu bulgu değerlendirilmiş olabilir) olmayanlardır. Uzman görüşüne göre, pupiller reflekslerle birlikte, korneal reflekslerin de olmayışı bu noktada kötü prognoz için belirleyicidir. Oküler refleksler ve SSPEs, hedef sıcaklıktan bağımsız olarak prediktif değerlerini korurlar.
Eğer kötü prognoz tahmininde yukarıdaki bulgulardan hiçbiri yoksa, bir grup daha az doğru tahmin ölçütleri değerlendirilebilir, fakat onların tahminlerdeki güvenirlik derecesi daha düşük olacaktır. Bunların FPR değeri
<%5’dir fakat daha önceki tahmin ölçütlerine göre daha geniş % 95 CIs sahiptir ve/veya prognoz belirleme çalışmalarındaki Tanım/eşik değerleri net değildir. Bu tahmin ölçütleri; erken status myoklonus (SDGD sağlandıktan sonraki 48 saat içinde), SDGD sağlandıktan sonraki 48-72 saat içindeki yüksek serum nöron spesifik enolaz (NSE), ısınma sonrasında reaksiyon vermeyen malign EEG tipleri (burst-supresyon, status epilepticus), belirgin azalmış gri cevher/beyaz cevher oranının (GM/WM) varlığı, veya SDGD sağlandıktan sonra 24 saat içinde sulkuslarda silinme veya SDGD sağlandıktan sonra 2-5 günde beyin magnetik rezonans görüntülemede (MRI) diffüz iskemik değişikliklerin varlığıdır. Uzman görüşüne dayanarak; ilk prognoz belirlenmesinden sonra, en az 24 saat beklemeyi ve ikinci prognoz belirleyicileri kullanmadan önce bilinci kapalı olanlarda Glasgow motor skorun 1-2 olduğunu teyid etmeyi önermekteyiz. Prognoz belirleme için bunların en az ikisinin birlikte olmasını öneririz.
Günümüzde kötü prognozu %0 FPR oranıyla tahmin eden spesifik bir NSE eşik değeri önerilememektedir. İdeal olanı, her hastanenin kendi kitlerini kullanarak NSE değerini çalışması ve kendi normal değerleri ile eşik değerini belirlemesidir. Farklı zaman dilimlerindeki örnekleme ile, NSE düzeylerinin trendlerinin saptanıp yanlış pozitif sonuç verme riskinin azaltılması önerilmektedir.
Çoğu çalışmalarda en güçlü belirteçler yanlış pozitif sonuçlar vermemekle birlikte, hiçbiri tek başına kesin doğrulukla kötü prognozu tahmin etmez. Dahası, bu belirleyiciler, tek başına karar verme riski ile birlikte,
yaşam sürdürme tedavisinin geri çekilmesi kararında sıklıkla kullanılmıştır. Bu nedenle, bunların bir tanesinin varlığında bile, eğer mümkün ise, prognoz belirleme için multimodal yöntemlerin kullanılmasını önermekteyiz. Güvenliği artırmanın yanısıra, kısıtlı kanıtlar multimodal prognoz tahmin yöntemlerinin sensitiviteyi de artırdığını düşündürmektedir.
Kesin olmayan bir sonuç ile meşgul olunduğunda, klinisyenler uzun süreli gözlemlerini dikkate almalıdır. Uzun süre klinik iyileşmenin olmayışı, kötü prognozu gösterir. Arrestten 25 gün sonra bile uyanma tanımlanmış olsa da, hayatta kalanların çoğunda bir hafta içinde bilinç açılır. Yakın zamanlı bir gözlemsel çalışmada, ısınmadan sonraki 4.5 gün içinde hastaların %94’ü, 10 gün içinde %6’sı uyanmıştır. Bu geç uyanmaya rağmen, iyi nörolojik sonuçlar hala olabilmektedir.
Rehabilitasyon
Kardiyak arrest sonrası yaşayanların büyük bir bölümü için, nörolojik sonuç iyi olarak değerlendirilse bile, bilişsel, emosyonel problemler ve bitkinlik yaygındır.452,492-494 Uzun süre bilişsel yetersizlik, özellikle hafif tipi, yaşayanların yarısında vardır.453,495,496 Hafif bilişsel problemler profesyonel sağlık bakımı ile sıklıkla tanınmazlar ve standart sonuç skalaları olan Serebral Performans Kategorileri (CPC) veya Mini Mental Durum Araştırmaları (MMSE) ile saptanamayabilirler. Bilişsel ve emosyonel problemlerin her ikisi de belirgin etkiye sahiptir ve hastaların günlük fonksiyonları ve iş ve yaşam kalitelerine geri dönmelerini etlileyebilir. Hastane taburculuğundan sonra, spesifik bir hemşire veya doktor ile sistematik bakımının yapılabileceği ortam sağlanmalıdır. Bilişsel yetersizlikler ve emosyonel problemler için en azından gözlemlenmiş olmalıdır ve bu konuda önceden bilgilendirilmelidir.
Organ bağışı
Organ bağışı, SDGD sağlanmış olan ve nörolojik değerlendirmeleri ile ölüm için tüm kriterleri sağlayan hastalarda düşünülmelidir. Yaşam destek tedavisinin geri çekilmesi kararı verilen komadaki hastalarda, organ bağışı, dolaşım ölümü meydana geldikten sonra değerlendirilmelidir. Organ bağışı, SDGD sağlamada KPR başarısız olduğunda da düşünülebilir. Organ bağışını ilgilendiren tüm kararlar, farklı zaman ve ortamlarda değişikliklere bağlı olarak lokal yasal ve etik gereklilikleri izlemelidir.
Kalıtımla geçmiş hastalıklar için tarama
Bir çok ani ölüm kurbanları, en sık koroner arter hastalığı olmak üzere, primer aritmi sendromu, kardiyomiyopati, ailesel hiperkolesterolemi ve prematür iskemik kalp hastalığı gibi sessiz yapısal kalp hastalıklarına sahiptir. Akrabaların primer korunması için kalıtsal hastalıklar için tarama yapmak, tıbbi izlem ve koruyucu anti-aritmik tedavi önemlidir.
Kardiyak arrest merkezleri
Kardiyak arrest ve resüsitasyon sonrası yaşamını sürdüren hastaların bakımı için çok çeşitli hastaneler vardır. Pek çok çalışma, kardiyak arrest merkezlerine transport ve hastaneden taburculuk arasında bir ilişki rapor etmiştir, fakat hasta sonuçları ile en çok ilişkili olan hastane faktörleri ile ilgili
belirsizlik vardır. Ayrıca bir kardiyak arrest merkezini oluşturan servislerle ilgili de belirsizlik söz konusudur. Uzmanların çoğu bir kardiyak arrest merkezinin 7/24 faaliyette olan kardiyak katetarizasyon laboratuvarına ve hedefli sıcaklık yönetimi sağlama olanaklarına sahip olması konusunda hemfikirdir.