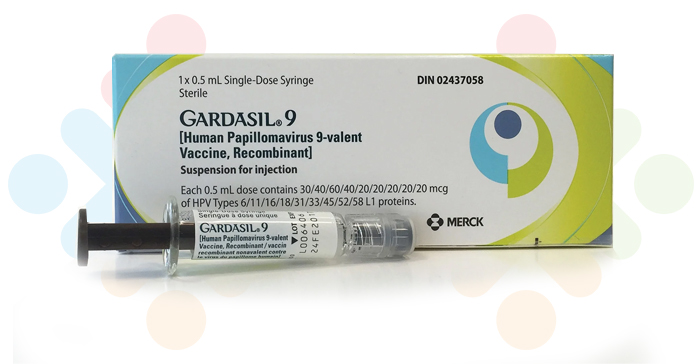
Gardasil, İnsan Papilloma Virüsünün (HPV) 9 tipine (6, 11, 16, 18, 31, 33, 45, 52, 58) karşı geliştirilmiş bir aşıdır.
GARDASIL 9 IM enjeksiyonluk süspansiyon 9-valan İnsan Papillomavirüs Aşısı [Tip 6, 11, 16, 18, 31, 33, 45, 52, 58] (Rekombinant, adsorbe)
- İlaç Adı : Gardasil
- Aşı Türü: Rekombinant
- Faz:
- Doz: 2-3 doz
- Uygulama Yeri: Deltoid veya uyluk kası İM
- Koruma Yüzdesi:
- Saklama Sıcaklığı: 2°C – 8°C arası sıcaklıklarda (buzdolabında)
- Saklama Yılı:
- Faz Çalışmalarına Katılan Ülkeler:
- Acil Kullanım İzni Aldığı Ülkeler:
- Bir doz (0,5 ml):
HPV1 Tip 6 L1 Proteini 2,3 30 mikrogram
HPV1 Tip 11 L1 Proteini 2,3 40 mikrogram
HPV1 Tip 16 L1 Proteini 2,3 60 mikrogram
HPV1 Tip 18 L1 Proteini 2,3 40 mikrogram
HPV1 Tip 31 L1 Proteini 2,3 20 mikrogram
HPV1 Tip 33 L1 Proteini 2,3 20 mikrogram
HPV1 Tip 45 L1 Proteini 2,3 20 mikrogram
HPV1 Tip 52 L1 Proteini 2,3 20 mikrogram
HPV1 Tip 58 L1 Proteini 2,3 20 mikrogram - Yaş: 9 yaşından itibaren İnsan Papillomavirüs (HPV) enfeksiyonunun neden olduğu
hastalıklara karşı korunmak için kullanılan bir aşıdır.
ENDİKASYONLAR
Gardasil 9, insan papilloma virüsünün (HPV) dokuz tipine (tip 6, 11, 16, 18, 31, 33, 45, 52 ve 58) karşı koruma sağlamak için 9 yaşından itibaren hem erkeklerde hem de kadınlarda kullanılan bir aşıdır. Bu virüslerin neden olduğu aşağıdaki durumlara karşı koruma sağlar:
- Rahim ağzı, vulva, vajina ve anüsteki kanser öncesi lezyonlar (büyümeler) ve kanserler,
- Genital siğiller.
MEKANİZMA
İnsan papilloma virüsleri (HPV), siğillere ve anormal doku büyümelerine neden olan virüslerdir. 100’den fazla papilloma virüsü türü vardır ve bunların bazıları hem erkeklerde hem de kadınlarda anogenital kanserlerle ilişkilidir. Rahim ağzı kanserlerinin neredeyse %100’ü HPV enfeksiyonlarından kaynaklanmaktadır. Avrupa’da, anal kanserlerin yaklaşık %90’ının, vulvar kanserlerin %15’inin, vajinal kanserlerin %70’inin ve penis kanserlerinin %30-40’ının HPV enfeksiyonuna bağlı olduğu tahmin edilmektedir. HPV tip 16 ve 18, rahim ağzı ve anal kanserlerin büyük çoğunluğuna neden olurken, HPV tip 6 ve 11, genital siğillerin çoğuna neden olmaktadır. Ek olarak, 5 HPV türü (31, 33, 45, 52 ve 58) de yüksek kanser geliştirme riski taşır (rahim ağzı kanserlerinin yaklaşık %20’sine neden olurlar).
Tüm papilloma virüsleri, ‘L1 proteinleri’ olarak adlandırılan proteinlerden oluşan bir kabuğa ya da ‘kapsid’e sahiptir. Gardasil 9, yukarıda belirtilen dokuz HPV türü için saflaştırılmış L1 proteinlerini içerir ve bu proteinler, ‘rekombinant DNA teknolojisi’ olarak bilinen bir yöntemle üretilir. Bu proteinler, vücudun kolayca tanıyabilmesi için HPV’ye benzeyen yapılar (virüs benzeri partiküller) olarak birleştirilir. Bu virüs benzeri partiküller enfeksiyon ya da hastalığa neden olma yeteneğine sahip değildir.
Aşı uygulandığında, bağışıklık sistemi L1 proteinlerine karşı antikorlar üretir. Aşılama sonrası, bağışıklık sistemi gerçek virüslere maruz kaldığında antikorları daha hızlı üretebilir. Bu da bu virüslerin neden olduğu hastalıklara karşı koruma sağlar.
Aşı ayrıca, daha iyi bir yanıtı teşvik etmek için alüminyum içeren bir ‘adjuvan’ (yardımcı madde) içerir.
Gardasil’in Araştırılması
Gardasil 9’un HPV enfeksiyonunun dokuz tipine karşı koruma sağlayabileceği, beş ana çalışmada gösterilmiştir. GARDASIL 9, 9-26 yaş arası erkeklerde ve 9 – 45 yaş arası kadınlarda çalışılmıştır.
- Birinci çalışma, 16-26 yaş arasındaki 14.000’den fazla kadın üzerinde Gardasil 9’un etkinliğini incelemiştir. Çalışmada, Gardasil 9 ile aşılanan kadınların, HPV tipleri 31, 33, 45, 52 ve 58’e bağlı hastalık (büyüme veya kanser) geliştirme olasılığı, daha önce onaylanmış ve HPV tipleri 6, 11, 16 ve 18’e karşı koruma sağlayan Gardasil aşısı ile karşılaştırılmıştır. Bu çalışma, 3 doz Gardasil 9 ile aşılanan 6.016 kadından yalnızca 1’inin, Gardasil ile aşılanan 6.017 kadından ise 30’unun HPV tipleri 31, 33, 45, 52 ve 58 ile ilişkili hastalık geliştirdiğini göstermiştir. Ayrıca, bu çalışma, Gardasil 9’un, HPV tipleri 6, 11, 16 ve 18’e karşı yeterli düzeyde antikor geliştirdiğini göstermiştir. Kadınlar, üçüncü dozdan sonra yaklaşık üç buçuk yıl boyunca izlenmiştir.
- İkinci çalışmada, 9-15 yaşlarındaki 3.066 kız ve erkek çocukta Gardasil 9’un etkisi, 16-26 yaşlarındaki genç kadınlardaki etkisiyle karşılaştırılmıştır. Ana etkililik ölçüsü, üçüncü dozdan bir ay sonra HPV tipleri 6, 11, 16, 18, 31, 33, 45, 52 ve 58’e karşı antikor gelişimiydi. Çalışma, aşının 9-15 yaş arasındaki kız ve erkek çocuklarda, 16-26 yaş arası kadınlar için hastalığa karşı koruma sağlandığı birinci çalışmada olduğu gibi, dokuz HPV tipine karşı yeterli düzeyde antikor üretimini teşvik ettiğini göstermiştir.
- Üçüncü çalışma, 9-15 yaş arasındaki 600 kız çocuğunda Gardasil 9’un etkisini, Gardasil ile karşılaştırmıştır. Çalışma, üçüncü dozdan bir ay sonra antikor gelişimini incelemiş ve Gardasil 9 ile aşılanan kız çocuklarının, Gardasil ile aşılanan kızlarla benzer düzeyde koruma sağladığını göstermiştir.
- Dördüncü ana çalışma, üçüncü dozdan bir ay sonra 16-26 yaş arası yaklaşık 1.419 genç erkekte ve 1.101 genç kadında dokuz HPV tipine karşı antikor düzeylerini karşılaştırmıştır. Bu çalışma, Gardasil 9’un hem genç erkeklerde hem de kadınlarda dokuz virüs tipine karşı benzer düzeyde koruma sağladığını bulmuştur.
- Beşinci ana çalışma, 1.518 kişi üzerinde, Gardasil 9’un iki dozluk bir programının etkisini üç dozluk bir programla karşılaştırmıştır. Çalışma, son dozdan bir ay sonra antikor gelişimini incelemiş ve iki doz Gardasil 9 verilen erkek ve kız çocuklarının, üç doz Gardasil 9 verilen kızlar ve kadınlarla benzer düzeyde koruma sağladığını göstermiştir.
Çalışmaların Sonuçları
Çalışmalar, Gardasil’in serviks kanserine neden olan HPV enfeksiyonlarına karşı etkili olduğunu göstermiştir. 9-14 yaş arasındaki kişilere verilen iki doz aşının, üç doz aşının sağladığı bağışıklık kadar etkili olduğu bulunmuştur.
Onaylanma Nedeni
EMA ajansın İnsan Kullanımı İçin Tıbbi Ürünler Komitesi (CHMP), Gardasil 9’un faydalarının risklerinden daha fazla olduğuna karar vermiş ve Avrupa Birliği’nde kullanım için onaylanmasını önermiştir. CHMP, Gardasil 9’un, önceki aşı Gardasil’den daha geniş bir kanser koruması sunduğunu değerlendirmiştir, çünkü HPV tipleri 16 ve 18’e ek olarak, daha az yaygın olan ancak yüksek risk taşıyan 5 yeni HPV tipine (31, 33, 45, 52 ve 58) karşı da koruma sağlar. Bu nedenle, Gardasil 9’un rahim ağzı, vajinal ve vulvar kanserlerin ve premalign lezyonların (kanser öncesi büyümeler) yanı sıra HPV ile ilişkili genital siğillerin çoğunu önlemesi beklenmektedir. Yan etkilere gelince, birçok hastada enjeksiyon bölgesinde reaksiyonlar gelişmesine rağmen, bu reaksiyonlar Gardasil ile olanlardan sadece biraz daha fazladır.
AŞI UYGULAMA
Gardasil 9, flakonlarda veya önceden doldurulmuş enjektörlerde bulunan enjeksiyonluk bir süspansiyondur. Gardasil 9, genellikle 9-14 yaş arası erkekler ve kızlar için iki dozluk veya üç dozluk bir programa, 15 yaş ve üzeri erkekler ve kadınlar için ise üç dozluk bir programa göre uygulanır. İki dozluk bir programda, ikinci doz, ilk dozdan beş ila on üç ay sonra yapılmalıdır. Üç dozluk bir programda ise, ikinci doz ilk dozdan iki ay sonra, üçüncü doz ise ikinci dozdan dört ay sonra yapılmalıdır. İlk doz ile ikinci doz arasında her zaman en az bir ay, ikinci doz ile üçüncü doz arasında ise en az üç ay olmalıdır ve tüm dozlar bir yıl içinde tamamlanmalıdır.
Gardasil 9’un ilk dozunu alan bireylerin, bu ilaç ile doz rejimini tamamlamaları önerilir. Aşı, kas içine enjeksiyon olarak uygulanır, tercihen omuz ya da uyluğa yapılır.

Cervarix, yaşa bağlı olarak iki veya üç doz şeklinde verilir:
- 9-14 yaş arası kişilere iki doz verilebilir. Bu dozlar, 1 ay arayla yapılır.
- 15 yaş ve üzeri olanlara ise üç doz verilir: Birinci ve ikinci doz arasında bir ay, ikinci ve üçüncü doz arasında beş ay olmalıdır.
- Kas içi (intramüsküler) enjeksiyon yapılır. Aşı omuz veya uyluk kasına İM enjeksiyon olarak verilir.
- 2ºC – 8ºC arası sıcaklıklarda (buzdolabında) saklanmalıdır. Kullanıma hazır enjektörü ışıktan korumak için kutusunda saklayınız. Aşı kesinlikle dondurulmamalıdır.
Renk değişikliği olması veya içinde yabancı maddeler bulunması durumunda aşıyı
kullanmayınız. GARDASIL 9 buzdolabından çıkarıldıktan sonra mümkün olan en kısa sürede uygulanmalıdır. Stabilite verileri aşı bileşenlerinin 8ºC ile 25ºC arasında veya 0ºC- 2ºC arasındaki sıcaklıklarda saklandığında 72 saat süreyle stabil kaldığını göstermektedir. Bu sürenin sonunda GARDASIL 9 kullanılmalı veya atılmalıdır. Bu veriler yalnızca geçici sıcaklık dalgalanmaları durumunda sağlık mesleği mensuplarına rehberlik etmek amacıyla sunulmaktadır. - Enjektörün saklanması esnasında saydam renksiz bir üst faz ile berrak beyaz bir çökelti
gözlenebilir. Bu bir bozulma belirtisi değildir. Enjektör içeriği aşıyı uygulamadan önce hem çalkalama öncesi, hem de çalkalama sonrası herhangi bir yabancı partikül ve/veya anormal fiziksel görünüm için görsel olarak incelenmelidir. Herhangi birinin gözlenmesi halinde, aşıyı kullanmayınız. - Kullanmadan önce aşı iyice çalkalanmalıdır.
- Bu aşı hiçbir zaman damar içi (intravenöz) veya cilt altı (subkutan) yoldan uygulanmamalıdır.
9-14 yaş aralığı (14 yaş dahil):
GARDASIL 9, 2 dozluk program önerilir.
- İlk enjeksiyon: Belirlenen bir tarihte
- İkinci enjeksiyon: İlk enjeksiyon sonrası 5 ve 13 ay arasındaki bir zamanda verilir
Eğer ikinci doz, ilk dozdan sonraki 5 aydan önce uygulanırsa, üçüncü doz mutlaka
uygulanmalıdır.
15 yaş ve üstü
GARDASIL 9, 3dozluk program önerilir.
- İlk enjeksiyon: Belirlenen bir tarihte
- İkinci enjeksiyon: İlk enjeksiyon sonrası 2 ay sonra (İlk dozdan sonra bir aydan önce
olmayacak şekilde) - Üçüncü enjeksiyon:
- İlk enjeksiyon sonrası 6 ay sonra (İkinci dozdan sonra 3 aydan önce
olmayacak şekilde)
Gerekli olduğu durumda aşılama takviminde esneklik yapılabilir ama üç dozun hepsi 1 yıl içerisinde verilmelidir.
Yaşlılarda kullanım:
Gardasil’in 45 yaşın üzerindeki erişkinlerdeki güvenliliği ve etkililiği incelenmemiştir.
YAN ETKİ
- Enjeksiyon bölgesinde: ağrı, kızarıklık, şişlik
- Baş ağrısıdır
- Kaslarda ağrı, hassasiyet veya güçsüzlük (egzersiz kaynaklı olmayan)
- Yorgunluk
- Bulantı, kusma, ishal ve karında ağrı dahil mide ve bağırsakla ilgili belirtiler
- Kaşıntı, deride döküntü, kurdeşen (ürtiker)
- Eklemlerde ağrı
- 38o C veya daha yüksek ateş
KAYNAKLAR
- https://titck.gov.tr/temizkt_b5a5bd92-9359-4139-95bc-b719238b3f98.pdf
- https://www.ema.europa.eu/en/medicines/human/EPAR/gardasil-9
İLGİLİ YAZI




















gardasıl d dımerı yukseltır mı bayılma senkop vertıgo yapar mı bazı ülkelerde yasaklanmış sebebi nedır
30 yaşta gardasil 9 ilk dozundan 2 ay sonra 2. dozu yapılıp üstünden 1 seneden fazla süre geçtiyse 3. doz yapılmalı mıdır? yoksa aşılamaya 3 doz baştan mı başlanmalıdır?
Gardasil 9 aşısında, dozlar arasındaki süre planlandığından uzun olsa da, aşılamaya kaldığınız yerden devam etmeniz genellikle yeterlidir. Yani, üçüncü dozu yaptırmak için yeniden baştan başlamanıza gerek yoktur; ikinci dozdan sonra geçen süreye bakılmaksızın yalnızca eksik kalan üçüncü dozu yaptırmanız önerilir.
Ancak, her durumda bir sağlık uzmanına veya doktorunuza danışarak, sizin özel durumunuza göre nasıl devam etmeniz gerektiğini netleştirmeniz en iyisidir.
Gardasil 9 aşısının bazı yan etkileri ve spekülasyonlar bulunsa da, bilimsel olarak güvenli olduğu ve ciddi yan etkilere nadiren yol açtığı bilinmektedir. Ancak, bazı bireylerde hafif ila orta düzeyde yan etkiler gözlenebilir:
1. D-dimer Seviyesi: Gardasil 9’un D-dimer seviyesini yükselttiğine dair kanıtlanmış bir bulgu yoktur. D-dimer, genellikle kan pıhtılaşmasıyla ilişkili bir belirteçtir, ancak HPV aşısı ile D-dimer artışı arasında bir ilişki kurulmamıştır.
2. Bayılma, Senkop ve Vertigo: Aşı sonrası bazı bireylerde bayılma veya senkop (ani bilinç kaybı) görülebilir. Bu durum, daha çok gençlerde ve enjeksiyon stresi ile bağlantılı olarak ortaya çıkabilir ve HPV aşısına özgü değildir. Bayılma eğilimi olan kişilerde aşı sonrası bir süre oturarak veya uzanarak beklemek tavsiye edilir. Vertigo (baş dönmesi) ise nadir olarak görülür.
3. Bazı Ülkelerde Yasaklanması: Gardasil 9, dünya genelinde birçok ülkede onaylanmıştır ve HPV’ye bağlı kanserleri önleme konusunda etkilidir. Ancak bazı ülkelerde, nadir de olsa ciddi yan etkilerle ilgili endişeler nedeniyle kısıtlamalar getirilmiştir. Bu ülkeler, genellikle aşının olası yan etkilerini yeniden değerlendirmek veya aşı konusunda şüpheye yol açan bireysel vakaları incelemek amacıyla sınırlamalar yapmıştır.
HPV aşıları konusunda Dünya Sağlık Örgütü (DSÖ) ve diğer büyük sağlık otoriteleri, Gardasil 9’un genel güvenli olduğunu ve faydalarının risklerinden çok daha ağır bastığını vurgulamaktadır. Aşı olmadan önce endişeleriniz varsa bir sağlık uzmanıyla konuşarak aşıyı yaptırmadan önce kapsamlı bilgi almak en sağlıklısıdır.